Un blog de ciencia para entender el funcionamiento del planeta y su relación con la historia de la humanidad
|
|
Hoy termino aquí mi "trilogía isotópica", aunque seguro que en el futuro seguiremos hablando de isótopos dada su importancia. Pero han sido tres entradas seguidas un poco más exigentes, en elaborarlas y en leerlas, por lo que la semana que viene volveré a curiosidades más ligeras, para poder acabar mi tesis y para no espantar a los pocos lectores que tengo. Hoy les explico la lógica detrás de las reconstrucciones de millones de años de la temperatura del planeta mediante el uso de los isótopos de oxígeno, método que fue por primera vez implementado en 1955 por Cesare Emiliani basándose en el trabajo de su mentor Harold Urey.
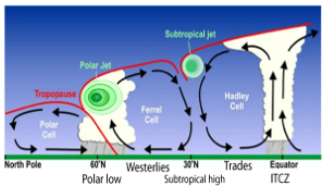
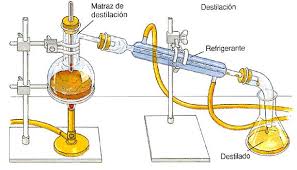
Vean la curiosa simetría entre las dos imágenes de arriba. A la izquierda es un esquema de la circulación atmosférica desde el ecuador hasta el polo norte. A la derecha tienen un destilador de laboratorio, cuyos principios fundamentales son los mismos que los destiladores del whisky, el tequila o el ron que os chupáis los fines de semana. En la parte central observamos dónde se calientan las masas líquidas. Vemos la zona del matraz de destilación donde una fuente de calor, el mechero de gas, está separando los líquidos del matraz según su punto de evaporación. Los líquidos más volátiles se evaporan antes que los menos volátiles. En el otro caso vemos la zona de convección de la atmósfera donde debido a una fuente de calor, el Sol, se produce la evaporación del agua. Al contrario que con la destilación en el matraz, para que se evapore el agua no hace falta que hierva a 100ºC como bien se explica en "ciencia de sofá". Al evaporarse el agua, se separan los isótopos del oxígeno; los isótopos ligeros al pesar menos se evaporan más fácil que los isótopos pesados.
Un paréntesis. Ya tuvimos una introducción a los isótopos donde utilizamos de ejemplo los isótopos del carbono. El oxígeno también presenta varios isótopos, el más abundante O-16 (8 protones y 8 neutrones) que es el ligero y el más pesado O-18 (8 protones y 10 netrones) y el cálculo del delta del oxígeno nos da resultados en el que un mayor delta significa que está enriquecido del isótopo pesado. Como saben el agua tiene hidrógeno y oxígeno (H2O) y el agua tiene tres isótopos principales, ya que el Hidrógeno también tiene sus isótopos (aquí muy buena revisión). Pero vamos a obviar al Hidrógeno y nos centraremos en la relación de H216O (el ligero) y H218O (el pesado).
Siguiendo con los paralelismos entre el destilador y la circulación atmosférica, vemos en ambos casos cómo desciende la fase gaseosa a la vez que se refrigera. Sin embargo, hay una diferencia, y es que en la circulación atmosférica durante el trayecto a zonas más frías parte va cayendo en forma de lluvia. ¿Adivinan qué isótopo va a caer antes? Efectivamente, el pesado, quien quiere llevar una carga pesada cuando puede llevar otra ligera del mismo valor ¿verdad?
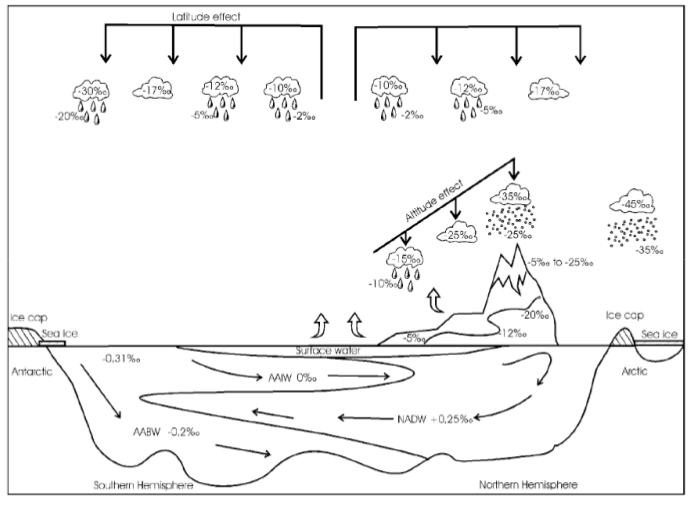
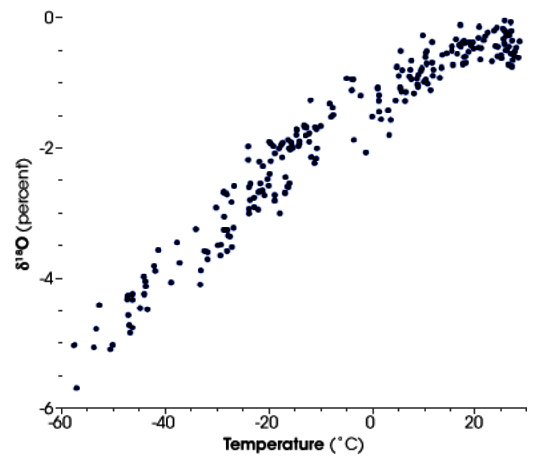
Al final del viaje todo el gas ha quedado condensado por el frío. En el matraz que recibe el destilado del tequila, primero llegará el alcohol más puro, el más volátil, en cierto modo el más ligero. En los polos, a través de la circulación atmosférica, lo que llegan son sobretodo isótopos ligeros en forma de nieve, la mayoría de los pesados fueron cayendo por condensación al enfriarse la atmósfera en el camino. El resultado es que el hielo de los polos tiene en promedio un delta del oxígeno menor que en la región tropical. Mientras lluvias tropicales tiene un delta de alrededor de -5%o, los glaciares de Groenlandia llegan a un delta de -30%o. El cero es el Promedio Estándar del Agua del Océano (SMOW en sus siglas en inglés). En la siguiente figura lo resumieron fantásticamente Paul y colaboradores en 1999.
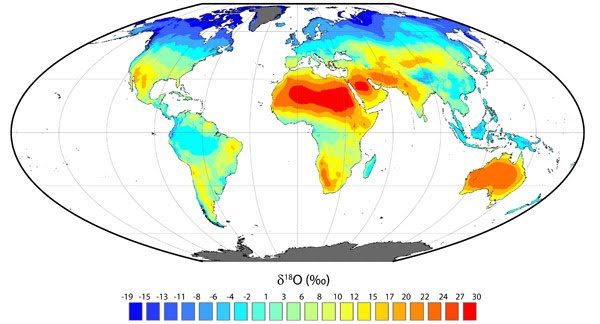
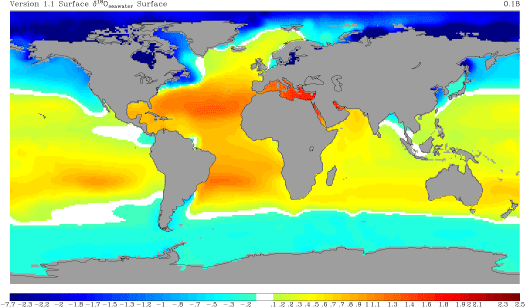
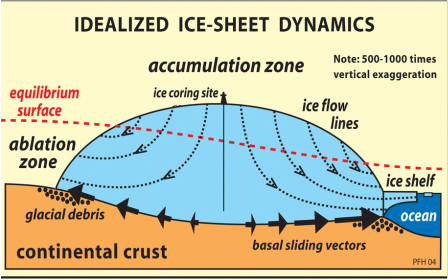
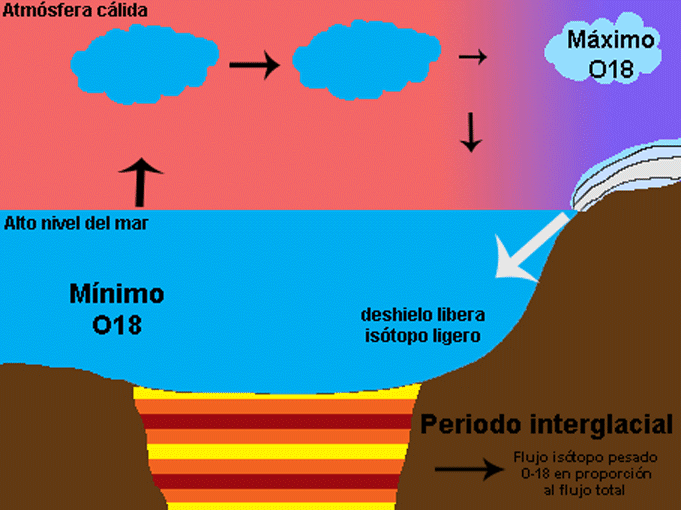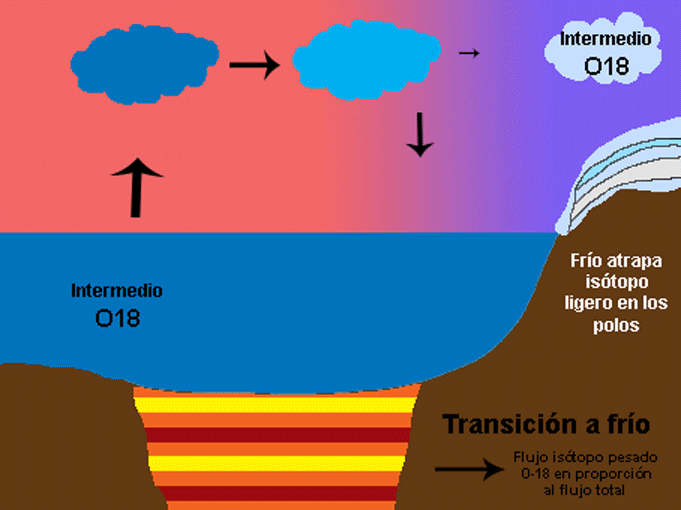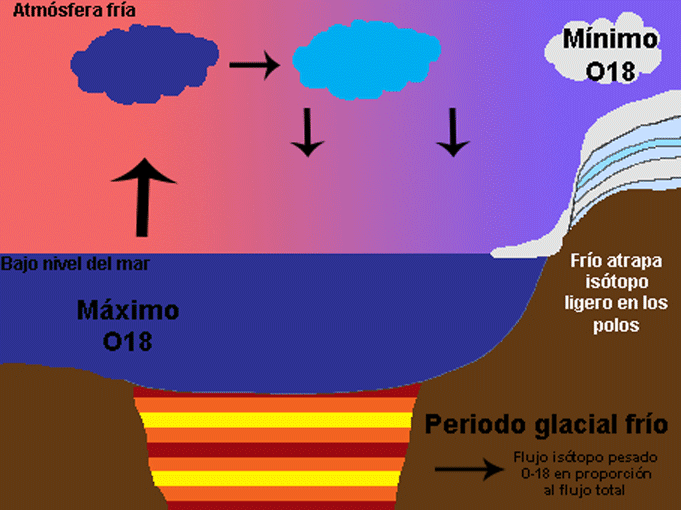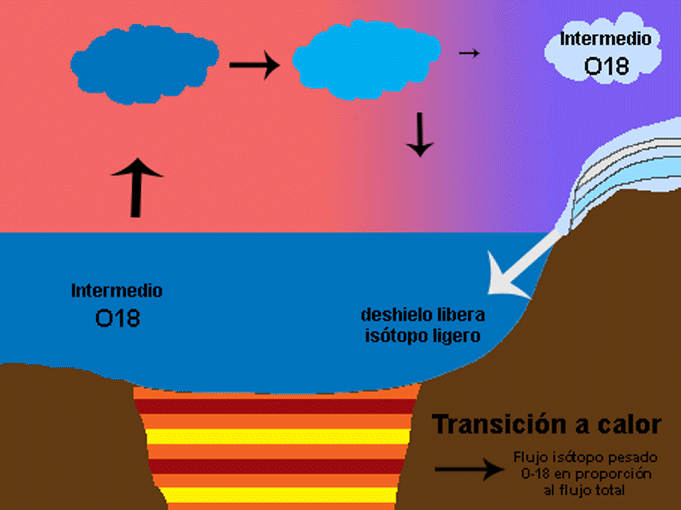
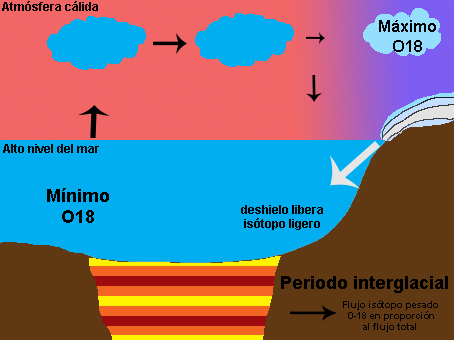
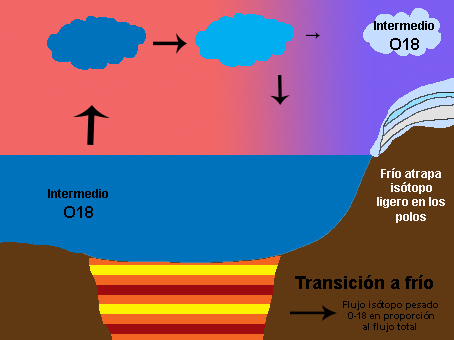
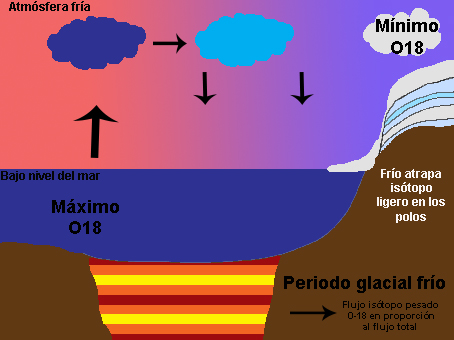
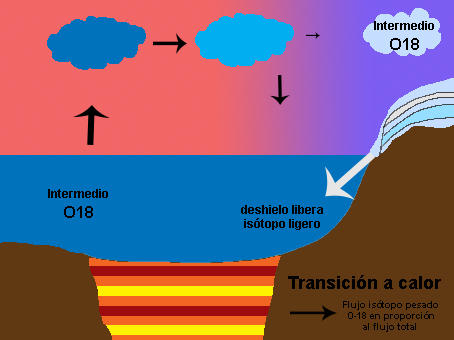
También hay que pensar no solo en el oxígeno que vuela, sino también en el que se queda. Así, zonas con mucha evaporación y muy secas, como los desiertos, presentan una proporción de isótopos pesados mucho mayor. En definitiva, el patrón global del delta 16 del oxígeno responde a la destilación del oxígeno y también al balance evaporación-precipitación local, como puede observarse en los mapas de abajo para los continentes (arriba) y el agua superficial del mar (abajo). La superficie del mar también sufre estos procesos, sus valores van desde -7%o a 3%o, pero debido a la mezcla sus rangos son mucho menores que en el medio terrestre, entre -20%o y 30%o. Pero hoy nos vamos a centrar en lo que es la destilación del oxígeno y la segunda parte del título de este artículo, la reconstrucción de la temperatura del planeta. Seguro que han oído muchísimas noticias sobre el deshielo de los polos o han visto esa película animada de “La edad de Hielo” que transcurre en un periodo del planeta bastante más frío que el actual. Ahora piensen por un momento cómo pueden esos periodos glaciales y cálidos afectar al contenido de isótopos de oxígeno en el hielo y en el mar. Para ello tengan en cuenta algo importante, los casquetes polares se descongelan por su parte inferior a la vez que la nieve se deposita en la parte superior. La relación del isótopo del oxígeno con las glaciaciones es muy sencilla. Cuando los casquetes polares tienen mucho hielo durante periodos fríos han acumulado isótopos ligeros. Esto quiere decir que en el mar quedan menos isótopos ligeros, y la relación 18O/16O aumenta, al igual que el delta del oxígeno, y el agua evaporada que viaja a los polos también tiene una mayor proporción de 18O. Sin embargo las condiciones frías llegan a latitudes más bajas lo que hace que durante el viaje a los polos se elimine todavía más isótopo pesado, quedando en los polos incluso mayor proporción de isótopo ligero. Lo contrario ocurre en periodos interglaciales. Bueno, es verdad, en realidad no es tan sencillo y a veces es un poco contraintuitivo. Así que vamos poco a poco. Les enseño una animación que he hecho y después lo explico paso a paso. Fíjense detenidamente cómo la señal no sólo queda registrada en el hielo de los polos, sino también en los sedimentos marinos. En éstos últimos, los isótopos de oxígeno quedan registrados en organismos como corales o con concha de carbonato de calcio, de los que ya hemos hablado antes (1 y 2) que cuando mueren caen al sedimento y se convierten en fósiles.
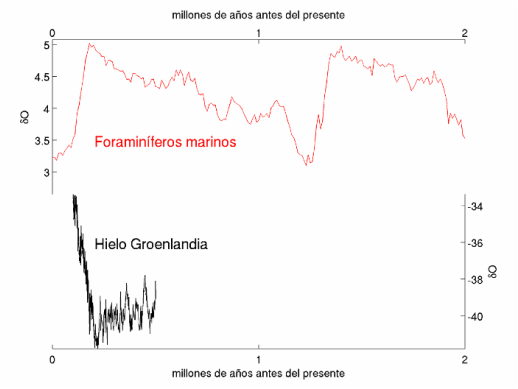
Ahora ya podemos entender porqué la señal isótopica del hielo y los de fósiles de sedimentos marinos es opuesta, uno es el espejo del otro como se ve en la figura de abajo. En el hielo, el máximo delta y la mayor cantidad de O18 es en periodo cálido, por lo que este delta es reflejo de la temperatura del planeta. En el caso del registro marino, el delta es el inverso de la temperatura del planeta.
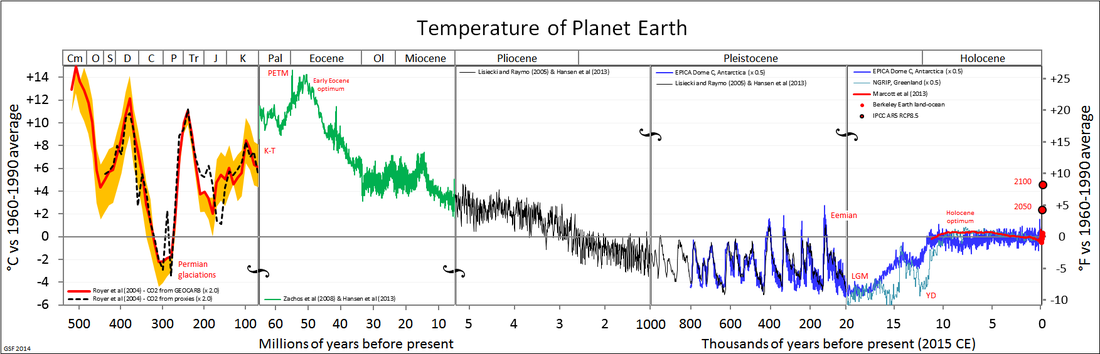
Como podéis ver también, los núcleos de hielo tienen mayor resolución y además son más fiables en la cronología, pero lo máximo que hay son 800000 años reconstruidos con el isótopo del Hidrógeno de un núcleo de la Antártida. En cambio los sedimentos nos permiten ir millones de años atrás. Algo que os puede llamar la atención son las diferencias en los valores del delta. Debéis tener en cuenta que al calcular el delta del oxígeno del hielo y agua se utiliza el estandar SMOW, pero para los carbonatos se utiliza otro estándar, el PDB que vimos aquí, por lo que no son un reflejo exacto de las diferencias del agua de mar y del hielo. Para reconstruir la temperatura a partir de los carbonatos marinos, hay que aplicar unas fórmulas obtenidas a partir de estudios de laboratorio, ya que la cinética de la reacción por la que se forma el carbonato de calcio, y en la que se incorporan los isótopos de oxígeno, varía con la temperatura. Pero, como decían en "Irma la dulce", esa es otra historia. Y ahora sí, os dejo con una reconstrucción de los últimos 500 millones de años a partir de diferentes proxys. Detalles acerca esta reconstrucción, aquí
*Si buscáis otras fuentes de información sobre este proceso no lo vais a encontrar de forma tan detallada como aquí en ningún material divulgativo, tanto en español como inglés, sólo en publicaciones más técnicas. Podéis buscar cosas relacionadas como isotopos del agua o paleotermómetro.
Un libro de la Agencia Internacional para la Energía Atómica y la UNESCO sobre todo lo que necesitas saber, y más, sobre isótopos en el ciclo hidrológico. [PDF]
0 Comentarios
Cuando se habla de evolución siempre se dice que sobreviven los animales que mejor se adaptan al medio, sin embargo esta afirmación tiene al menos una excepción, el Homo sapiens, es decir, nosotros los humanos. El éxito de los humanos se basa en su capacidad de transformar el medio a sus intereses, capacidad que muy pocos otros animales tienen (se me ocurre el castor, que hace embalses para criar de forma segura a su prole) y desde luego ninguno a la escala de transformación que ha conseguido el humano. Hoy voy a relataros la historia que nos cuentan los isótopos de carbono en el Este de África, de cómo el cambio de clima transformó la sabana y con ello el devenir de la humanidad en un grupo de homínidos anteriores al H. sapiens que fue capaz de aprovechar los recursos de muy diversas fuentes. Todavía no transformaban el medio a sus necesidades, pero desde luego fue un primer paso en esa dirección.
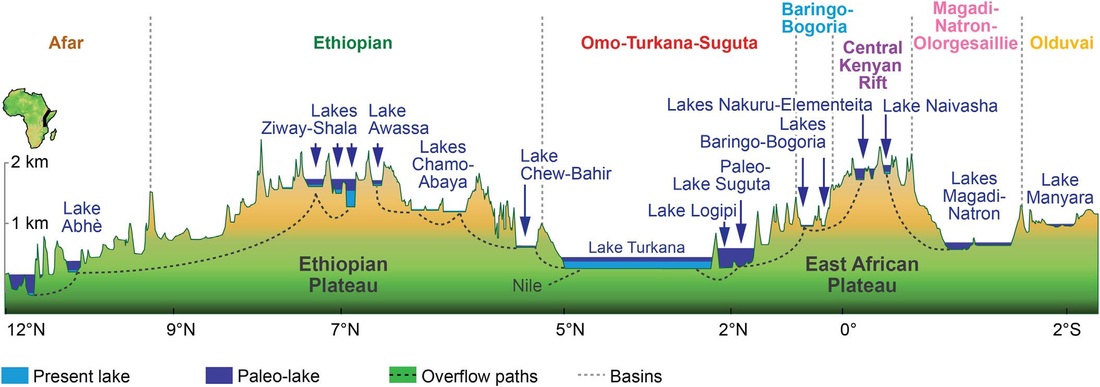
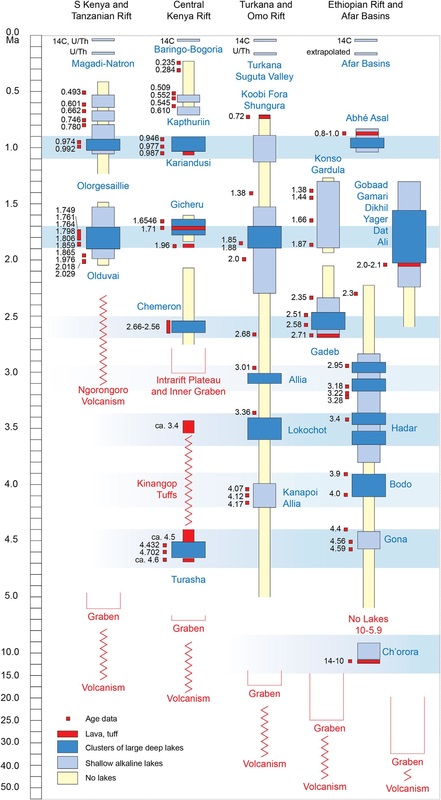
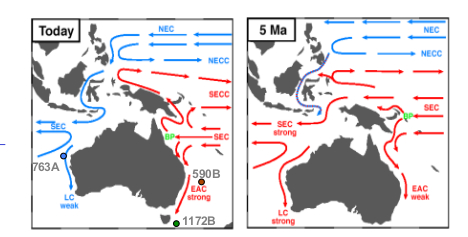
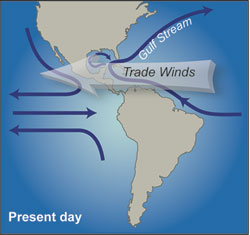
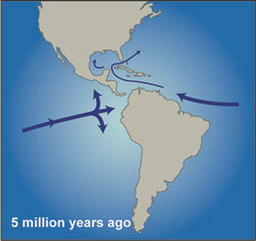
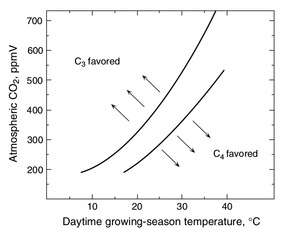
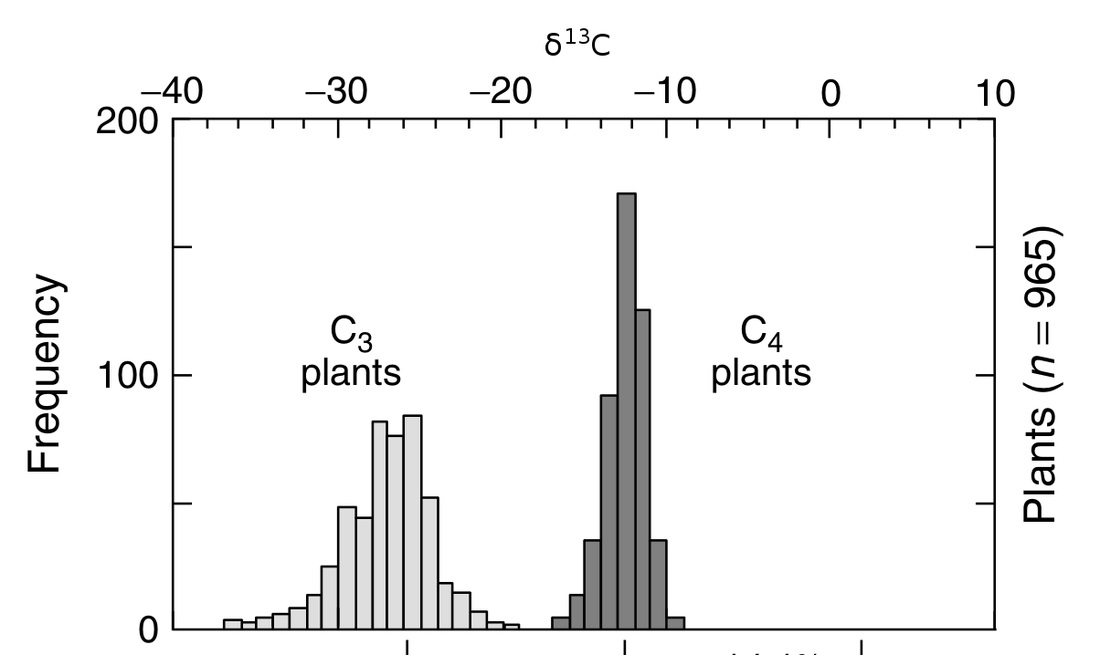
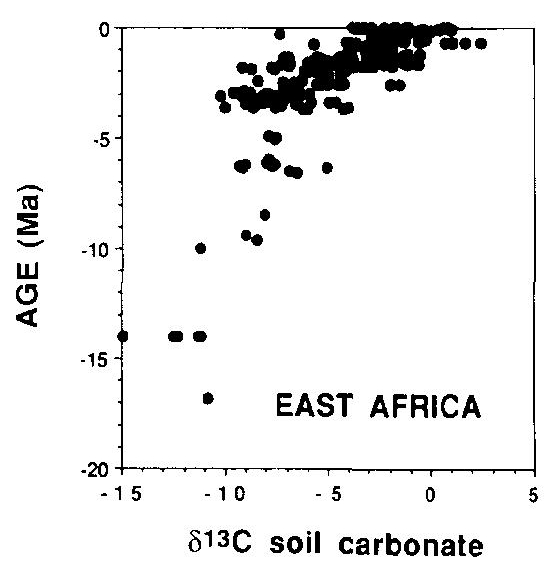
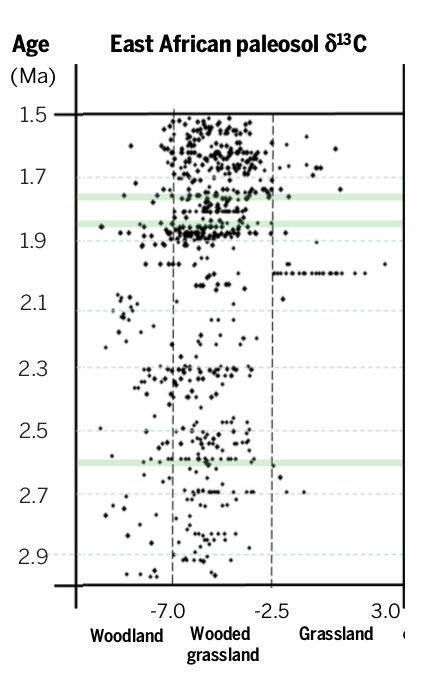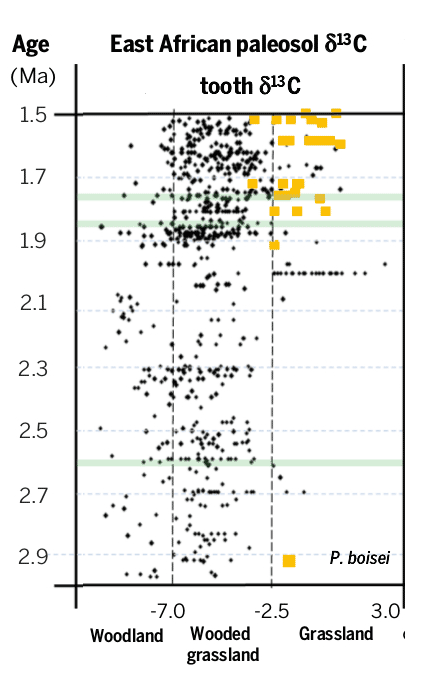
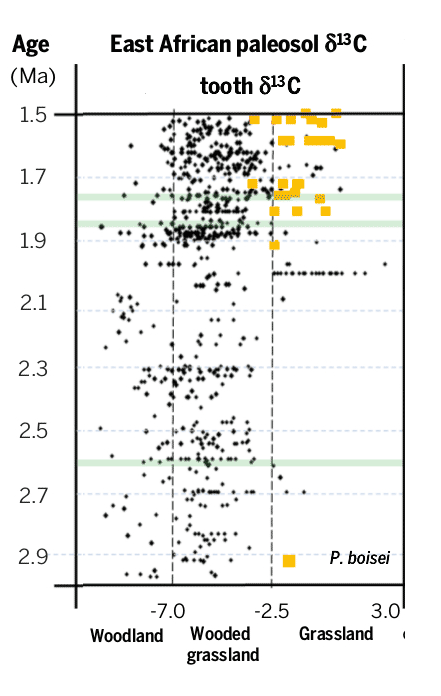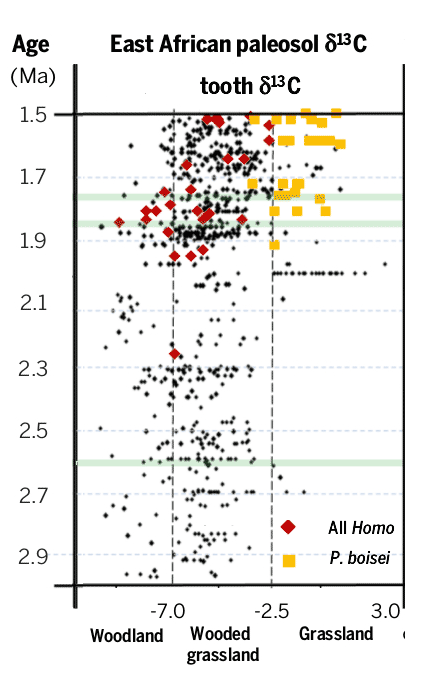
Esta alta variabilidad monzónica se superpuso a una larga tendencia que desde hace entre 3 y 10 millones de años el Este de África se ha ido haciendo más seco y árido. Este rango de fechas es tan amplio porque ni si quiera se está seguro cual fue el proceso que produjo ese lento cambio, aunque en todas las hipótesis coinciden en un tipo de forzamiento del que todavía no hemos hablado, el producido por el movimiento de las placas tectónicas, por ejemplo el choque de continentes o el levantamiento de cordilleras. Y si todavía no había hablado de este tipo de forzamiento no es porque no sea importante, sino porque todavía no había hablado de escalas de millones de años, pero tengan claro que son el tipo de cambio que más ha modificado el clima a lo largo de la historia del planeta. Como pueden imaginar este tipo de cambios son lentos y su efecto en el clima son a largo plazo, aunque en ocasiones pequeños cambios en la disposición de los continentes pueden producir enormes cambios climáticos. Hay tres hipótesis principales, que no se excluyen mutuamente, para explicar la aridificación del Este de África: 1º Cambios tectónicos en la zona del Rift Africano. Esta es la parte sur del Gran Rift que se extiende hasta Asia. La parte Africana es una abertura que recorre desde el mar Rojo hasta Mozambique que nos indica que dos placas tectónicas se están separando y se calcula que en 10 millones de años lo harán completamente. Esta zona está llena de grandes lagos que acogieron a los primeros humanos y es precisamente los estudios de formación de nuevos lagos y la desaparición de otros los que más apoyan esta hipótesis (Maslin y colaboradores). 2º Cambios tectónicos en los estrechos de Indonesia. La conexión de los océanos Pacífico e Índico a través de las islas de Indonesia tiene una enorme importancia en el clima global. Los registros geológicos muestran cambios en este archipiélago hace alrededor de 3 millones de años. Estos cambios habrían producido que el flujo principal cambiase del sur al norte, es decir, en el Índico empezó a entrar más agua del Pacífico norte en vez del ecuador y el sur, lo que produjo un enfriamiento en el Índico. Los modelos climáticos muestran cómo este cambio de temperatura en el Índico habría producido el incremento de las condiciones áridas en el Este de África (Cane y Molnar 2001) 3º El cierre del Istmo de Panamá y la unión de América del Norte y América del Sur. Esto produjo un cambio en la circulación oceánica tanto en el Atlántico, activando la corriente del Golfo, como en el Pacífico comenzando las condiciones actuales con una corriente ecuatorial con alta productividad marina en el Este del Pacífico tropical. Algunos piensan que este incremento en la productividad pudo ser tan importante como el cambio en el flujo de calor por el cambio en las corrientes marinas y atmosféricas asociadas (también empezó la circulación de Walker que está relacionada con El Niño), ya que capturaría una gran cantidad de CO2 atmosférico que a la larga produciría un enfriamiento. Este evento se considera como uno de los más importantes de los últimos 60 millones de años* y seria el responsable del inicio de los ciclos de glaciaciones que empezaron hace 3 millones de años. A favor de esta hipótesis es que los cambios en la vegetación fueron globales y no exclusivos del Este de África (Cerling y colaboradores). En la figura inferior los cambios en la circulación con el cierre del Istmo de Panamá. Imagen de http://www.whoi.edu/ Sea cual sea la o las causas iniciales, lo cierto es que en el Este de África el medio se empezó a hacer más árido en la escala de millones de años, pero con gran variabilidad de periodos húmedos y secos en la escala de miles de años. La hipótesis más aceptada de la evolución humana, y que ya casi suena a leyenda, es que el cambio de zona boscosa a la sabana africana favoreció a los monos que tenían una posición erguida para alejarse de forma segura de la zona arbórea. Cuando nos imaginamos esta postal pensamos en la actual sabana africana, con esos pastos altos que dominan sitios míticos como el Serengueti o Masai Mara. Sin embargo esos pastos todavía no dominaban el ecosistema de la sabana cuando aparecieron los monos erguidos por aquellos lugares. La sabana de entonces debía ser bastante más boscosa de lo que es hoy, aunque sin duda ya existían algunas zonas donde dominaban los pastos. Esto lo sabemos gracias a la señal de isótopos de carbono que han dejado las plantas en los paleosuelos.
Actualmente somos la única especie de hominino (homínido con caminar erguido) que existe. Sin embargo hace millones de años eramos varias las especies de monos caminantes que existían y convivían. Visto que ahora quedamos sólo nosotros probablemente no convivíamos de forma muy pacífica. Si nos vamos a hace aproximadamente de 2 a 3 millones de años en el registro fósil, vemos que es el momento en el que surgieron los generos Homo y Paranthopus a partir de los Australopitecus, género este último a la que pertenecía la mítica Lucy. Estas fechas coinciden con la aparición de las primeras herramientas de piedra, esencialmente unas piedras afiladas a base de golpes y, como hemos visto, con el cambio hacia condiciones áridas en el Este de África. 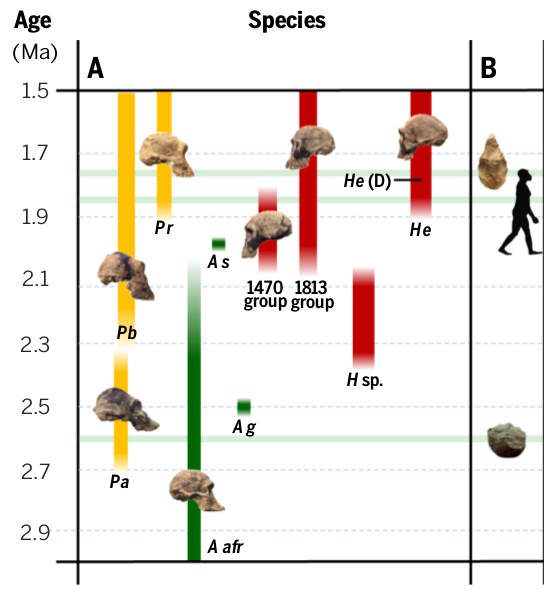 Evolución de los homininos hace entre 3 y 1.5 millones de años. Los que empiezan por A, son Austrlopitecus. Los que empiezan por P, son Paranthopus. Los que empiezan por H son del género Homo. A la derecha aparece las fechas de dos tipos de herramientas para cortar, mucho más avanzada la de hace 1.7 millones de años. Alrededor de 1.8 millones de años se marca la primera gran dispersión del género Homo fuera de África. De Antón y colaboradores 2014
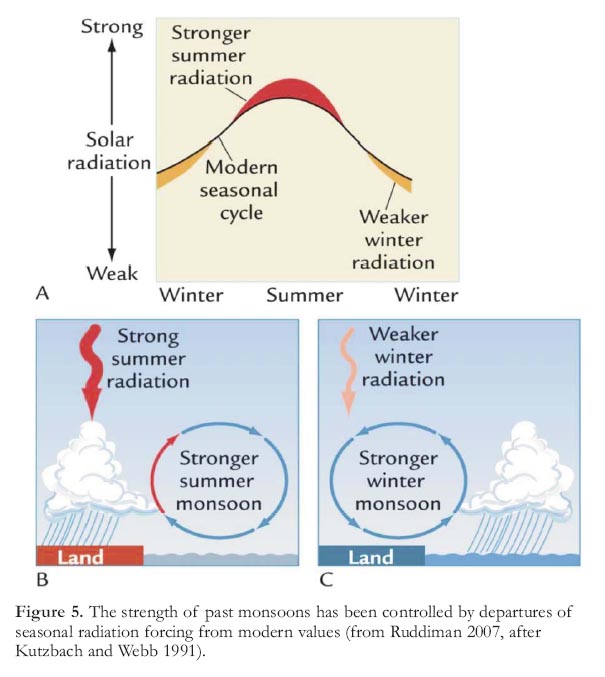
Hay que recordar que sobre la tendencia de cada vez condiciones más áridas, se superponía una gran variabilidad monzónica debido a las variaciones orbitales. Estas condiciones cambiantes sin duda no debían favorecer a una especie tan especializada como Paranthopus, que terminó extinguiéndose hace alrededor de un millón de años. Probablemente tampoco le favoreció la presencia de otras especies del género Homo que en ese periodo amplió enormemente su capacidad craneal. Las especies del género Homo demostraron su capacidad de sobrevivir a condiciones cambiantes, y hoy estamos aquí produciendo nosotros mismos los cambios en el planeta. ¿Seremos capaces de sobrevivir a nuestros propios cambios? * Sólo otros dos eventos se consideran de una importancia similar al cierre del Istmo de Panamá en los últimos 60 millones de años. El choque del continente indio con Eurasia y el consecuente levantamiento del Himalaya, y la separación de la Antártida y el inicio de la corriente circumpolar Antártica, que mantiene a la Antártida congelada y aislada climáticamente. ** En realidad hay un tercer grupo, las plantas CAM que representan un porcentaje menor comparado con las C3 y C4. Este texto (y este otro) está claramente inspirado por una de esas conferencias que uno recuerda con cierta predilección. La dio Peter de Menocal en la AGU del 2014 y pueden verla en este enlace de youtube. Todo el crédito para él. Aquí un minicongreso para profundizar en el tema organizado por deMenocal
Aunque he seguido los lineamientos que propone deMenocal, lo cierto es que en este tema se está lejos de un verdadero consenso. Hay algunos autores que ponen en duda un papel tan importante del clima en la evolución humana, o que el cierre del Istmo de Panamá fuese hace 3 millones de años, o que los cambios en el Este de África empezaron mucho antes, etc. A continuación les dejo dos revisiones en inglés por si quieren profundizar y el enlace a wikipedia en español sobre la evolución humana. También pueden revisar los numerosos enlaces a estudios que he dejado a lo largo del texto. Maslin et al., 2014 [PDF] 17 páginas Kingston 2007 [PDF] 40 páginas Evolución humana
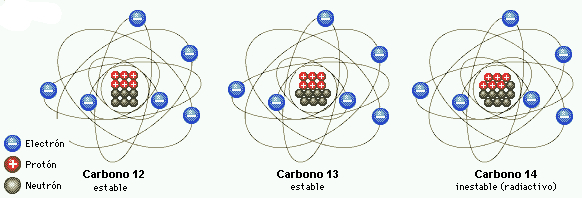
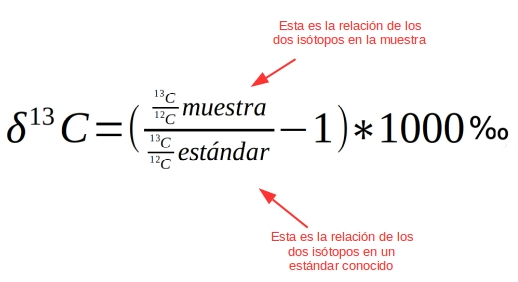
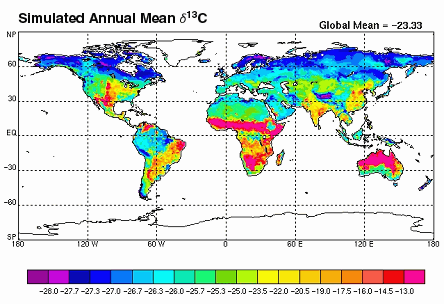
 Ya hace un tiempo expliqué cómo las cosas se transforman y se convierten en proxys (o las convertimos en proxys) con el ejemplo del cementerio de Atari, donde se enterraron los juegos de ET. Uno de los proxys más utilizados en paleociencia son los isótopos, pero probablemente a muchos eso de isótopos les suene a chino. Si viajamos 3 horas desde el cementerio de Atari hasta Albuquerque, podremos ir a ver un partido de los Isótopos de Albuquerque, el equipo que le robó el nombre al equipo preferido de Homer Simpson, los isótopos de Springfield, y que ahora existe en la vida real. Si veían los Simpsons recordarán que el equipo se llamaba así por la central nuclear, ya que estas instalaciones utilizan los isótopos radiactivos para obtener energía. Espero que con este recordatorio de los Simpsons no os suene tan a chino. En cualquier caso, intentaré ser claro en la introducción de hoy al tema de los isótopos. Espero, queridos lectores, no se asusten si me pongo a hablar de átomos o neutrones y se animen a leerlo, porque los isótopos son una puerta a un mundo apasionante. Por ejemplo, gracias a los isótopos de carbono sabemos cuándo fue el momento clave en que el Homo sapiens, es decir, nosotros, se seleccionó evolutivamente sin tener que adaptarse a un único medio, sino explotando los recursos de diferentes ecosistemas. O también cómo el viaje de los átomos del oxígeno por la atmósfera nos cuenta las variaciones del clima del planeta. Historias que podréis leer a partir de la semana que viene. También he hablado de isótopos en historias anteriores (1, 2, 3) Si hacemos memoria, un átomo tiene protones, neutrones y electrones. Los protones y los electrones tienen carga eléctrica, positiva y negativa respectivamente, y su número es lo que identifica al átomo. Así, si utilizamos el Carbono como ejemplo, éste tiene 6 protones y 6 electrones. Sin embargo, aunque suelen tener también 6 neutrones, a veces puede tener más, 7 u 8. Sigue siendo Carbono, pero son unos isótopos más pesados de Carbono. El Carbono 12 (6 protones +6 neutrones le da masa = 12) y el Carbono 13 (6 p +7 m = 13) son isótopos estables; el C12 es el isótopo ligero y el C13 es el isótopo pesado. También está el Carbono 14 (6+8=14) que es inestable porque tiene un número de neutrones que provoca grandes tensiones en el átomo. A los isótopos inestables se les conoce como isótopos radiactivos, como los de las centrales nucleares, y tienden a convertirse en isótopos estables. Para ello puede seguir varios caminos, por ejemplo atrayendo electrones y protones, expulsándolos, convirtiendo los neutrones en protones, etc. En el caso del C14 se convierte en un isótopo estable de Nitrogeno con masa 14 al ganar un electrón y convertir un neutrón en protón. Así, por ejemplo, en un pedazo de madera tendremos una gran cantidad de C12 y un poco de C13 y C14. Lo interesante es que el contenido de C14 va disminuyendo a lo largo de los años porque es inestable y lo hace a un ritmo constante lo que nos permite utilizarlo como un cronómetro en cuenta regresiva. Cuanto menos C14 tenga ese trozo de madera, significa que es más antiguo. Por eso la famosa prueba de carbono 14 para muestras de origen orgánico que seguro han visto en algún programa de la tele. El problema es que llega un momento que todo el C14 se gasta y no es posible datar con C14 material orgánico de más de 50000 años, por lo que hace falta otros elementos radiactivos con vida más larga (técnicamente mayor periodo de semidesintegración) u otro tipo de aproximaciones para datar los materiales. Otro día haré un especial de técnicas de cronología. En cualquier caso estos isótopos radiactivos no sólo se utilizan para datar, sino que también pueden ser en sí mismos un proxy. Por ejemplo, el C14 en anillos de árboles es un buen proxy de la actividad solar, como las tormentas solares de las que ya hablamos aquí. El caso de los isótopos estables tiene más matices, y lo que cambia y se utiliza como proxy es la relación entre dos isótopos estables de un mismo elemento referido a un estándar conocido. En el caso del Carbono, el C12 y el C13. Siguiendo con el ejemplo del Carbono a esa proporción la llamamos "delta 13 del Carbono" o simplemente "delta del Carbono", y se calcularía de esta manera: Uno de los estándares de C más usados es de los fósiles de cefalópodos Belemnitas de la formación Pee Dee. Una formación geológica del Cretácico descrita en el río Pee Dee de Carolina del Sur, en USA. Estos fósiles tienen una excepcionalmente elevada relación 13C/12C y se utiliza como el cero. Fotos: http://www.blackriverfossils.org/FlorenceCounty/tabid/53/TripReports/753/Default.aspx Para entender cómo y porqué cambia la relación de estos isótopos, y su respectivo "delta", pondré un ejemplo. Imagínese una persona con un cheque de un millón de dólares, va al banco a cobrarlo y le dicen que puede escoger cómo se lo lleva: puede escoger desde una enorme bolsa con un millón de dolares llena de monedas de un céntimo a una mochila con un millón de dolares en billetes de 100 dolares. ¿Cual se llevaría? Los dos valen lo mismo, pero seguro que preferiría la mochila porque pesa menos y se la llevaría y utilizaría más fácilmente. Ahora imagine que después llega otra persona con otro cheque de un millón de dólares, pero los del banco le dicen que ya no tiene tantos billetes de 100 dolares y que se tendrá que llevar parte en otros billetes y monedas más pequeñas, lo que aumenta el peso y la dificultad de transportarlo y utilizarlo. Si llegase una tercera persona con un cheque de un millón de dolares, el director del banco le diría que sólo le quedan billetes pequeños y monedas (y le preguntaría dónde reparten cheques de un millón de dolares como si fuesen caramelos). Este proceso es lo que se denomina fraccionamiento, ya que se está fraccionando en grupos de diferente peso un mismo recurso, el dinero del banco. Ahora imaginen que los tres afortunados con el cheque son en realidad una banda de estafadores, y cuando llegan a su guarida mezclan el botín y lo vuelven a repartir en volúmenes y pesos similares. Ese es el proceso de mezcla, y tanto el fraccionamiento como la mezcla son los dos procesos que gobiernan la distribución de los diferentes tipos de monedas/billetes. Al final tendríamos dos grupos diferenciados debido al fraccionamiento y la mezcla; un grupo que serían los estafadores, y otro grupo que sería el banco, que se quedó con todas las monedas más pesadas. Algo similar ocurre con la “elección” que hacen los procesos físicos, químicos y biológicos con los isótopos estables; pueden utilizar ambos isótopos, pero siempre preferirán el isótopo ligero y desecharán el pesado porque es más “cómodo” de transportar y utilizar, a no ser de que ya sólo queden isótopos pesados disponibles para utilizar. En el fondo el fraccionamiento no es más que una cuestión de gasto energético. Por otra parte la naturaleza tiene la manía de revolver las cosas, mezclándolas. El balance entre fraccionamiento y mezcla de los isótopos tiene unas enormes implicaciones a nivel ambiental, ya que ha dibujado a nivel global patrones de circulación atmosférica, marina, mapas de vegetación, etc. En la siguiente imagen tienen una modelación de la distribución del delta del Carbono en los continentes, que depende esencialmente de cómo distintos tipos de plantas captan y utilizan el CO2 atmosférico bajo diferente disponibilidad de agua. Pero eso lo veremos en detalle otro día. Hasta aquí la introducción a los isótopos. Sólo añadir que el uso de isótopos no es exclusivo de las paleociencias, ya que también se usan en en otras áreas como ecología, agricultura o medicina. Enlaces a wikipedia en español para profundizar en la física de los isótopos estables y radiactivos. Si tienen un buen nivel de inglés consulten mejor la versión inglesa de la wikipedia: Carbono-14 Radiactividad y decaimiento radiactivo Isótopos estables |
Archivos
Noviembre 2017
Categorías
Todos
|





 Fuente RSS
Fuente RSS