Un blog de ciencia para entender el funcionamiento del planeta y su relación con la historia de la humanidad
|
Climáticamente tiene una importancia enorme ya que el calor puede quedar guardado en el océano profundo o ser liberado cuando sube a superficie. Pero de eso hablaremos la semana que viene. Hoy contaremos qué es eso de la circulación termohalina, y para terminar con el tema de las cronologías, veremos su efecto en las dataciones con radiocarbono.
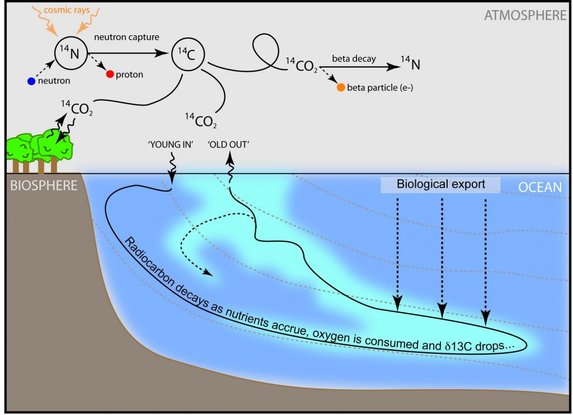
Existen algunas zonas donde se mezclan estas capas, las zonas donde el agua se hunde y las zonas donde el agua surge hacia superficie ¿y qué puede hacer que un agua que está en superficie se hunda?, el frío polar. Así, las aguas que provienen del Golfo de México, cálidas y relativamente saladas, y se dirigen hacia el polo norte, por la corriente del golfo, cuando llegan a la altura de Islandia y Groenlandia se enfrían. Como tienen una cantidad de sales mayor que las aguas de lluvia de Norteamérica y norte de Europa, se hunden hasta el fondo. Este proceso de hundimiento puede ser mayor o menor según la formación de hielo marino y su extensión, ya que al formar los cristales de hielo se expulsa la sal, la cual queda en el agua líquida, formando una masa de agua de muy alta salinidad que se hundirá todavía más rápido. Algo parecido ocurre en algunos puntos de la Antártida, donde ya vimos en este video de la BBC el caso extremo en el que un hundimiento de aguas salinas y muy frías iba dejando una columna helada. Estas zonas de hundimiento se consideran los motores de la circulación termohalina y donde comienza un viaje que se calcula puede durar hasta mil años. Evidentemente, si en un sitio está entrando agua, en otro tiene que salir. Las aguas que se hundieron en el Atlántico norte viajan por el fondo, se juntan con las de la Antártida que son incluso más densas, y ambas masas de agua se ponen a dar vueltas alrededor de la Antártida hasta que en un momento se desvían hacia el Pacífico y el Índico en dirección al ecuador. En este viaje hacia el ecuador se van calentando y van subiendo hacia la superficie ayudadas por la orografía, ya que en el camino se van topando con montañas submarinas, islas, etc que les ayuda a surgir. Una vez en superficie, finalmente, las corrientes superficiales cerrarán el ciclo llevándolas hasta al Atlántico Norte. Si nos ponemos a pensar en el C14 radiactivo que hay en la atmósfera y entra en el agua podemos deducir que cuanto mayor tiempo haya estado en el fondo una parcela de agua, menor contenido de C14 va a tener, ya que se interrumpe la llegada de C14 nuevo y el que ya estaba va decayendo radiactivamente. Así, a priori podemos calcular la edad del agua, entendiendo que ese agua “nace” cuando se aleja de la atmósfera. La diferencia de edad radiocarbono entre la medida en cada lugar y la atmosférica es lo que se llama “edad de reservorio” y se utiliza para hacer las pertinentes correcciones en dataciones de fósiles de sedimentos marinos. Generalmente las mediciones se hacen en conchas, ya que la señal de C14 que incorpora un organismo al construir la concha es la misma que tiene el agua, y a ser posible de organismos que viviesen antes de las primeras bombas atómicas o incluso antes de la quema de combustibles fósiles, para que que no interfiera en la proporción de C14. Es decir, fundamentalmente de colecciones antiguas y museos. Uno podría pensar que la edad de las aguas superficiales va a ser cero, ya que hay un equilibrio químico con la atmósfera, pero lo cierto es que hay muchas interferencias en la señal de C14. Los propios procesos físicos relacionados con el viento que hacen surgir aguas subsuperficiales de otras masas de agua, mezclando señales de C14 . También el fitoplancton (microalgas marinas) fija C14 que lo incorpora al ecosistema y este ecosistema no es estático y muchos organismos migran verticalmente, mezclando señales de C14 de capas de agua diferentes. O incluso el vulcanismo submarino incorpora grandes cantidades de carbono sin ningún tipo de radiactividad, alterando la proporción C12/C14.
Como pueden imaginar esto tiene muchas imprecisiones y es el talón de Aquiles de las reconstrucciones con sedimentos marinos que suelen manejar fechas con amplios márgenes de error (por ejemplo, en mis estudios de la corriente de California + 50 años). A parte de las razones ya mencionadas, la circulación termohalina puede ser más rápida o lenta según la velocidad de hundimiento, por el clima, la cantidad de hielo, etc, por lo que las edades reservorio habrán cambiado a lo largo de los siglos y milenios. Así que tenemos dos incógnitas, la edad del fósil y la edad reservorio, pero una sola variable, una medición de C14 A veces hay suerte y puede calcularse las variaciones de esa edad reservorio en escalas miles de años gracias a las sintonizaciones orbitales de las que ya he hablado antes. Por ejemplo, tomamos un núcleo de sedimento de una región, medimos una variable que sabemos varía con las variaciones orbitales, como el isótopo de oxígeno, y también medimos el C14 de conchas de foraminíferos que quedaron atrapados en el sedimento. Primero sintonizamos el isótopo de oxígeno con la variación orbital para darle una edad y así nos queda la medición de C14 para calcular la edad reservorio. Este es más menos el ejercicio que realizaron en aguas de Perú y que pueden ver en la imagen inferior, 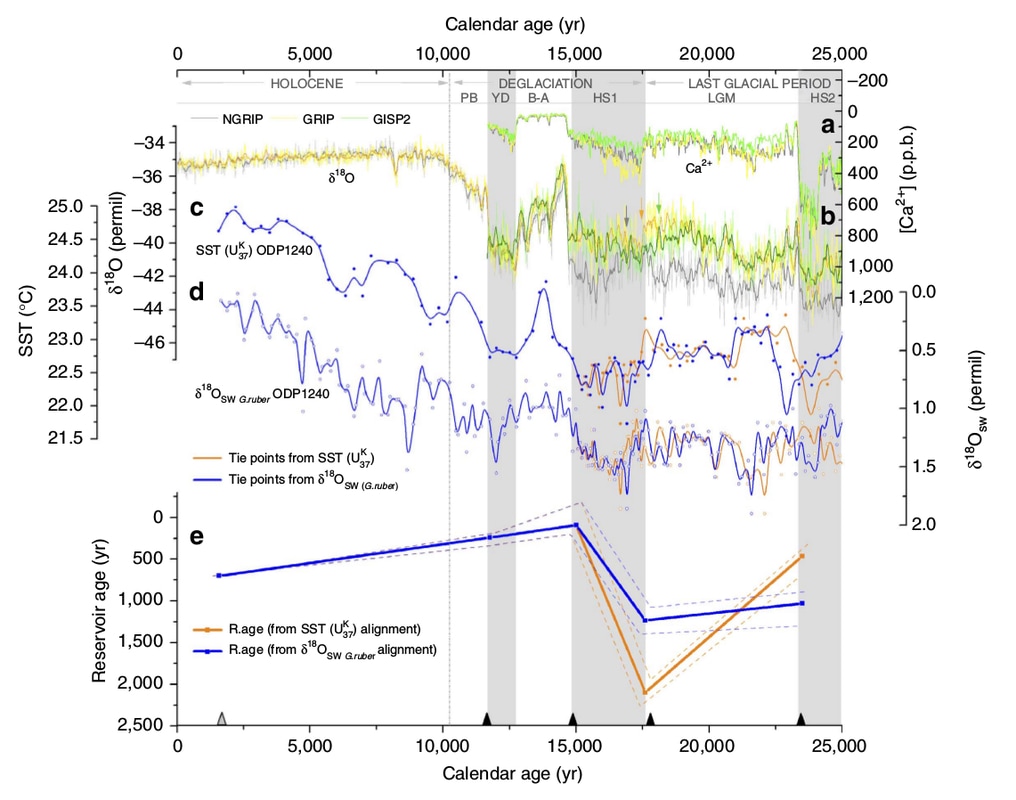 de arriba a abajo; registros del hielo de Groenladia en amarillo y verde; después dos regstros de temperatura e isotopo de oxígeno que en la gran escala es similar al planetario y por lo tanto se sintoniza con el registro de Groenlandia. Abajo del todo, las dos posibles variaciones de edades de reservorio según la sintonización utilizada. Click en la foto para ver Fuente y colaboradores, 2015
Referencias y enlaces de interés: Sobre circulación termohalina hablaré más la semana que viene. Hay muchas páginas con explicaciones de esta circulación, por ejemplo en wikipedia Sobre edades de reservorio no hay mucho en español, creo que esta entrada es bastante completa a nivel divulgativo y no conozco otra. En la wikipedia en inglés viene un buen resumen de los reservorios de edad con el C14 La "biblia" de referencia: Radiocarbon Software para cálculos de edades radiocarbono Para explorar edades de reservorio en google Earth Aquí podéis ver en qué consiste el truco del buzo, no es más que unos buzos cabeza abajo en un lago helado
0 Comentarios
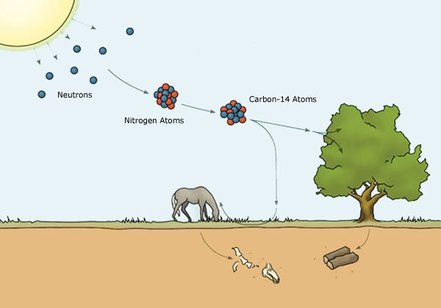
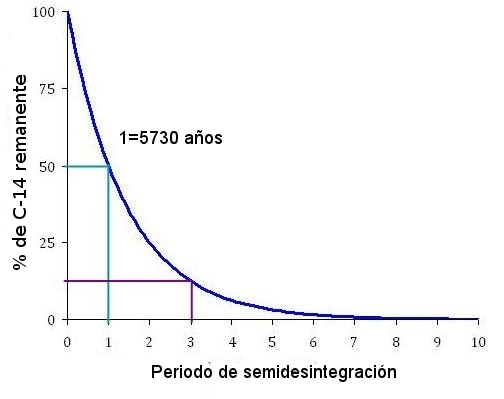
Ahora bien, dependiendo de que tipo de objeto sea y de su edad, deberemos utilizar un tipo u otro de radioisótopo. Los materiales más recientes se datan con la famosa técnica del carbono 14, de la que ya hablamos un poco, y para entenderlo primero les contaré un poco el ciclo de ese carbono radiactivo. El isótopo radiactivo del carbono 14 (C-14) se produce en la atmósfera, cuando los rayos solares impactan en las capas superiores. Este impacto hace que se introduzca un neutrón en un átomo de nitrógeno (con 7 protones y 7 neutrones) y a la vez salga un protón, resultando en un átomo de C-14 (con 6 protones y 8 neutrones). Estos átomos de C-14 entran en el ciclo de la vida a través de la fotosíntesis de las plantas, ya que la base de cualquier organismo es el carbono. Un organismo integrará C-14 en una proporción similar a la presente en la atmósfera hasta el día que muera. Una vez muerto, o al menos sin actividad vital como una semilla, empieza a perder isótopos de carbono radiactivo sin incorporar nuevos; ese C-14 vuelve a ser un átomo de Nitrógeno y empieza una cuenta atrás que utilizamos como cronómetro y que deja de funcionar cuando ya no quedan átomos de C-14.
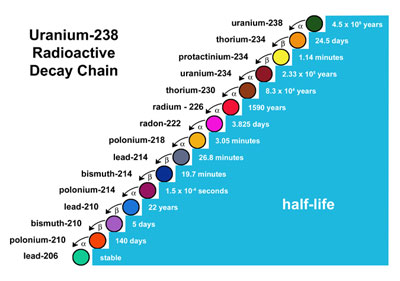
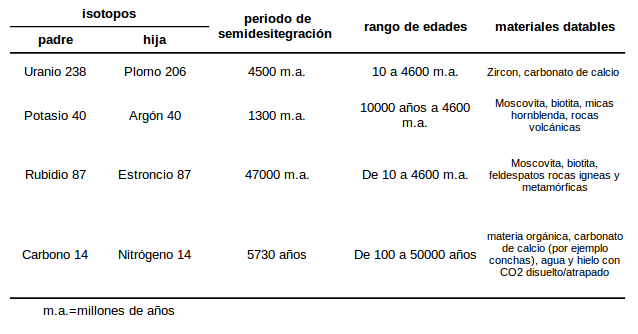
Sin embargo la complicación viene en donde medirlo. Por ejemplo, los fósiles de dinosaurio fueron hueso hace mucho tiempo pero al fosilizar se convierten en roca, y no presenta ningún elemento radiactivo que nos pueda informar de sus edad. Así, si encontramos un diente de Tyranosaurus rex, necesitaremos encontrar un material datable cercano a ese fósil. Y aquí viene el más difícil todavía; mientras que los fósiles se encuentran en materiales sedimentarios, la mayoría de materiales datables, son de origen volcánico, y metamórficos, rocas que ya han tenido un proceso de comprensión y calentamiento en el manto terrestre (ve tabla abajo). Es aquí donde entran las técnicas no absolutas de las que hablé anteriormente e incluso las sintonizaciones orbitales. Para tener cronologías fiables es fundamental tener unos buenos mapas geológicos donde tengamos claro cómo se relacionan las diferentes capas estratigráficas, la presencia de antiguas explosiones volcánicas, de su geomagnetismo, etc, a través de extensas regiones geográficas. Así, para datar un fósil, puedes estar utilizando un zircón encontrado a kilómetros de donde estaba el fósil. Si se fijan bien en la tabla, hay un periodo de tiempo, entre hace 50000 y 100000 años que no queda bien representado por ninguna de las dataciones. Es por eso que los dientes de los Arvicolinos se han convertido en un método de datación tan importante (llamado en la jerga el vole-clock) ya que aporta una precisión razonablemente buena a los fósiles de ese periodo de tiempo. Hay otras técnica de datación absoluta tanto a nivel atómico, luminiscencia o la resonancia del spin de los electrones, como moleculares, principalmente orgánicos como aminoácidos*, que cada día se utilizan más, y que en ocasiones cubren periodos de tiempo o materiales sedimentarios que no cubren los radioisótopos.
El ADN también puede servir y se utiliza en temas evolutivos como edades absolutas, pero no da una fecha más o menos exacta, así que yo la consideraría más bien un método de datación relativo.
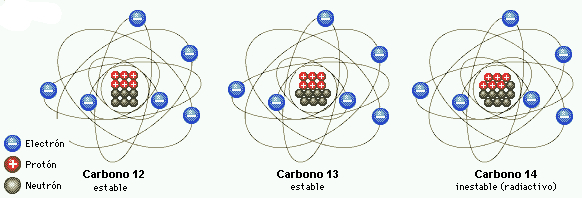
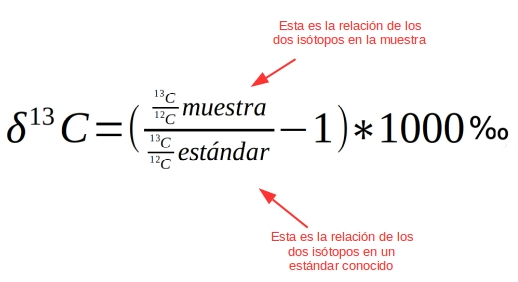
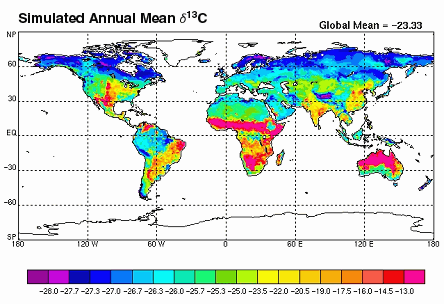
 Ya hace un tiempo expliqué cómo las cosas se transforman y se convierten en proxys (o las convertimos en proxys) con el ejemplo del cementerio de Atari, donde se enterraron los juegos de ET. Uno de los proxys más utilizados en paleociencia son los isótopos, pero probablemente a muchos eso de isótopos les suene a chino. Si viajamos 3 horas desde el cementerio de Atari hasta Albuquerque, podremos ir a ver un partido de los Isótopos de Albuquerque, el equipo que le robó el nombre al equipo preferido de Homer Simpson, los isótopos de Springfield, y que ahora existe en la vida real. Si veían los Simpsons recordarán que el equipo se llamaba así por la central nuclear, ya que estas instalaciones utilizan los isótopos radiactivos para obtener energía. Espero que con este recordatorio de los Simpsons no os suene tan a chino. En cualquier caso, intentaré ser claro en la introducción de hoy al tema de los isótopos. Espero, queridos lectores, no se asusten si me pongo a hablar de átomos o neutrones y se animen a leerlo, porque los isótopos son una puerta a un mundo apasionante. Por ejemplo, gracias a los isótopos de carbono sabemos cuándo fue el momento clave en que el Homo sapiens, es decir, nosotros, se seleccionó evolutivamente sin tener que adaptarse a un único medio, sino explotando los recursos de diferentes ecosistemas. O también cómo el viaje de los átomos del oxígeno por la atmósfera nos cuenta las variaciones del clima del planeta. Historias que podréis leer a partir de la semana que viene. También he hablado de isótopos en historias anteriores (1, 2, 3) Si hacemos memoria, un átomo tiene protones, neutrones y electrones. Los protones y los electrones tienen carga eléctrica, positiva y negativa respectivamente, y su número es lo que identifica al átomo. Así, si utilizamos el Carbono como ejemplo, éste tiene 6 protones y 6 electrones. Sin embargo, aunque suelen tener también 6 neutrones, a veces puede tener más, 7 u 8. Sigue siendo Carbono, pero son unos isótopos más pesados de Carbono. El Carbono 12 (6 protones +6 neutrones le da masa = 12) y el Carbono 13 (6 p +7 m = 13) son isótopos estables; el C12 es el isótopo ligero y el C13 es el isótopo pesado. También está el Carbono 14 (6+8=14) que es inestable porque tiene un número de neutrones que provoca grandes tensiones en el átomo. A los isótopos inestables se les conoce como isótopos radiactivos, como los de las centrales nucleares, y tienden a convertirse en isótopos estables. Para ello puede seguir varios caminos, por ejemplo atrayendo electrones y protones, expulsándolos, convirtiendo los neutrones en protones, etc. En el caso del C14 se convierte en un isótopo estable de Nitrogeno con masa 14 al ganar un electrón y convertir un neutrón en protón. Así, por ejemplo, en un pedazo de madera tendremos una gran cantidad de C12 y un poco de C13 y C14. Lo interesante es que el contenido de C14 va disminuyendo a lo largo de los años porque es inestable y lo hace a un ritmo constante lo que nos permite utilizarlo como un cronómetro en cuenta regresiva. Cuanto menos C14 tenga ese trozo de madera, significa que es más antiguo. Por eso la famosa prueba de carbono 14 para muestras de origen orgánico que seguro han visto en algún programa de la tele. El problema es que llega un momento que todo el C14 se gasta y no es posible datar con C14 material orgánico de más de 50000 años, por lo que hace falta otros elementos radiactivos con vida más larga (técnicamente mayor periodo de semidesintegración) u otro tipo de aproximaciones para datar los materiales. Otro día haré un especial de técnicas de cronología. En cualquier caso estos isótopos radiactivos no sólo se utilizan para datar, sino que también pueden ser en sí mismos un proxy. Por ejemplo, el C14 en anillos de árboles es un buen proxy de la actividad solar, como las tormentas solares de las que ya hablamos aquí. El caso de los isótopos estables tiene más matices, y lo que cambia y se utiliza como proxy es la relación entre dos isótopos estables de un mismo elemento referido a un estándar conocido. En el caso del Carbono, el C12 y el C13. Siguiendo con el ejemplo del Carbono a esa proporción la llamamos "delta 13 del Carbono" o simplemente "delta del Carbono", y se calcularía de esta manera: Uno de los estándares de C más usados es de los fósiles de cefalópodos Belemnitas de la formación Pee Dee. Una formación geológica del Cretácico descrita en el río Pee Dee de Carolina del Sur, en USA. Estos fósiles tienen una excepcionalmente elevada relación 13C/12C y se utiliza como el cero. Fotos: http://www.blackriverfossils.org/FlorenceCounty/tabid/53/TripReports/753/Default.aspx Para entender cómo y porqué cambia la relación de estos isótopos, y su respectivo "delta", pondré un ejemplo. Imagínese una persona con un cheque de un millón de dólares, va al banco a cobrarlo y le dicen que puede escoger cómo se lo lleva: puede escoger desde una enorme bolsa con un millón de dolares llena de monedas de un céntimo a una mochila con un millón de dolares en billetes de 100 dolares. ¿Cual se llevaría? Los dos valen lo mismo, pero seguro que preferiría la mochila porque pesa menos y se la llevaría y utilizaría más fácilmente. Ahora imagine que después llega otra persona con otro cheque de un millón de dólares, pero los del banco le dicen que ya no tiene tantos billetes de 100 dolares y que se tendrá que llevar parte en otros billetes y monedas más pequeñas, lo que aumenta el peso y la dificultad de transportarlo y utilizarlo. Si llegase una tercera persona con un cheque de un millón de dolares, el director del banco le diría que sólo le quedan billetes pequeños y monedas (y le preguntaría dónde reparten cheques de un millón de dolares como si fuesen caramelos). Este proceso es lo que se denomina fraccionamiento, ya que se está fraccionando en grupos de diferente peso un mismo recurso, el dinero del banco. Ahora imaginen que los tres afortunados con el cheque son en realidad una banda de estafadores, y cuando llegan a su guarida mezclan el botín y lo vuelven a repartir en volúmenes y pesos similares. Ese es el proceso de mezcla, y tanto el fraccionamiento como la mezcla son los dos procesos que gobiernan la distribución de los diferentes tipos de monedas/billetes. Al final tendríamos dos grupos diferenciados debido al fraccionamiento y la mezcla; un grupo que serían los estafadores, y otro grupo que sería el banco, que se quedó con todas las monedas más pesadas. Algo similar ocurre con la “elección” que hacen los procesos físicos, químicos y biológicos con los isótopos estables; pueden utilizar ambos isótopos, pero siempre preferirán el isótopo ligero y desecharán el pesado porque es más “cómodo” de transportar y utilizar, a no ser de que ya sólo queden isótopos pesados disponibles para utilizar. En el fondo el fraccionamiento no es más que una cuestión de gasto energético. Por otra parte la naturaleza tiene la manía de revolver las cosas, mezclándolas. El balance entre fraccionamiento y mezcla de los isótopos tiene unas enormes implicaciones a nivel ambiental, ya que ha dibujado a nivel global patrones de circulación atmosférica, marina, mapas de vegetación, etc. En la siguiente imagen tienen una modelación de la distribución del delta del Carbono en los continentes, que depende esencialmente de cómo distintos tipos de plantas captan y utilizan el CO2 atmosférico bajo diferente disponibilidad de agua. Pero eso lo veremos en detalle otro día. Hasta aquí la introducción a los isótopos. Sólo añadir que el uso de isótopos no es exclusivo de las paleociencias, ya que también se usan en en otras áreas como ecología, agricultura o medicina. Enlaces a wikipedia en español para profundizar en la física de los isótopos estables y radiactivos. Si tienen un buen nivel de inglés consulten mejor la versión inglesa de la wikipedia: Carbono-14 Radiactividad y decaimiento radiactivo Isótopos estables |
Archivos
Noviembre 2017
Categorías
Todos
|







 Fuente RSS
Fuente RSS